质粒构建(五步学会质粒构建原理)
质粒构建是分子生物学研究中最常用的实验技术。原百思特网理依赖于限制性核酸内切酶,DNA连接酶和其他修饰酶的作用,分别对目的基因和载体DNA进行适当切割和修饰后,将二者连接在一起,再导入宿主细胞,实现目的基因在宿主细胞内的正确表达。
质粒构建方式多样,常规的T4连接酶,下面就介绍下T4连接酶构建质粒方法,T4连接酶可用于平末端也可用于粘性末端连接,但一般推荐适用黏性末端。
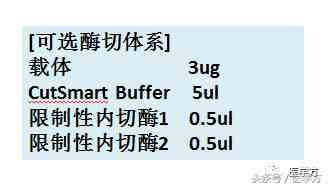
补水至50ul,37C孵育3~4小时,每隔一段时间振荡一下并离心以防液滴蒸发至管盖上。酶切后载体通过切胶回收线性化载体。
双酶切1和2,在设置酶切体系时要考虑酶切温度以及 Activity in NEBbuffer的问题,可在NEB公司主页的Double Digest Finder里面进行查询。
(1)引物设计方法:举个栗子,比如选择的限制性内切酶为BglII与HindIII,则根据酶切位点序列在引物的两端加粘性末端碱基序列。


引物合成形式:5’-GATCNNNNNNNNNNNNNNNNNNNN-3’
3’-NNNNNNNNNNNNNNNNNNNNTCGA-5’
(2)在PCR仪中按照以下touch down程序运行95C, 5 min; 95–85C at −2C /s; 85–25C at −百思特网0.1C /s; hold at 4C。

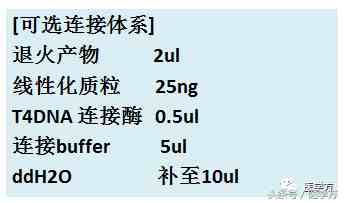
T4 DNA酶百思特网连接一般选择 16℃过夜。
注:连接可以选择公式计算,一般按照最适克隆载体与插入片段摩尔比为1:2,即最适插入片段使用量为0.06 pmol。这些摩尔数对应的DNA质量可由以下公式粗略计算获得:
最适克隆载体使用量 = [0.02克隆载体碱基对数]ng (0.03 pmol)
最适插入片段使用量 = [0.04插入片段碱基对数]ng (0.06 pmol)
将连接产物转化到受体菌中(一般为DH5a),涂板,培养过夜。注意质粒的抗性,选择对应的平板。
挑去平板上的单克隆培养,可以通过PCR或者酶切初步鉴定阳性克隆,对初步
鉴定出来的阳性克隆进行测序。